- Рак печени: дистанционная лучевая терапия
- Обширное отторжение слизистой оболочки тонкой и толстой кишки у пациента с тяжелой формой COVID-19
- Инфекция тонкого кишечника человека, вызванная SARS-CoV-2, характеризуется инфильтрацией слизистой оболочки активированными CD8 + Т-клетками
- COVID-19: биологическая и иммуносупрессивная терапия в гастроэнтерологии и гепатологии
- Фиброз печени как причина более низкого ответа на вакцину COVID
- Распространенность COVID-19 у пациентов с аутоиммунным заболеванием печени в Европе: онлайн-опрос, ориентированный на пациентов
- Исследование предполагает, что утрата кишечного эпителиального барьера является основной причиной мультисистемного воспалительного синдрома у детей
- Частота встречаемости заболеваний желудочно-кишечного тракта и печени, связанных с употреблением алкоголя, резко возросли во время пандемии
- Влияние COVID-19 на аномалии печени: систематический обзор и метаанализ
- COVID-19 и заболевание печени: механистические и клинические перспективы
- Редкий случай гетеротопического панкреатита и мальротации кишечника у пациента, инфицированного COVID-19. COVID-19 - причина или совпадение?
- Острые поражения желудочно-кишечного тракта и пищевая непереносимость как прогностические факторы тяжелобольных пациентов с COVID-19
- Желудочно-кишечные проявления, связанные с заражением SARS-COV-2: симптомы аппендицита (описание клинического случая)
- Последствия COVID-19 для гастроэнтеролога
- Микробиом полости рта связан с диагнозом COVID-19
- Характеристики желудочно-кишечных симптомов у пациентов с тяжелой формой COVID-19: систематический обзор и метаанализ
- Влияние терапевтического средства на микробную экосистему (MET-2) на рецидивирующую инфекцию Clostridioides difficile : открытое исследование фазы 1 в одной группе
- Повышенная передача сигналов через TLR / MyD88 у пациентов с ожирением: есть ли связь с тяжестью заболевания COVID-19?
- Новое понимание физиопатологии COVID-19: SARS-CoV-2-ассоциированное желудочно-кишечное заболевание
- Клинический случай пациента с трансплантацией печени в анамнезе с инфекцией COVID-19 с благоприятным исходом
- Кишечная непроходимость, вздутие, ишемия - колит, спровоцированный COVID-19: разбор клинического случая и обзор литературы
- Новые доказательства повреждающего действия COVID-19 на печень
- Последствия COVID-19 для занятого гастроэнтеролога
- Развязывая узел: острое кровотечение из варикозно расширенных вен у пациента с COVID-19. О чем следует помнить гастроэнтерологу?
- COVID-19 и печень: обзор
- Влияние повреждения печени на стратификацию риска и ведение пациентов с COVID-19
- Covid-19 и повреждение печени: систематический обзор
- COVID-19: аномальные тесты функции печени
- COVID и печень
- Клинические особенности функциональной аномалии печени, связанной с COVID-19
- Клинические особенности и потенциальный механизм поражения печени, связанного с коронавирусной болезнью 2019 г.
- Изучение механизма использования матрина в лечении COVID-19 в сочетании с повреждением печени с помощью сетевой фармакологии и технологии молекулярного докинга
ЖКТ и гепатобилиарная система
Кислородное обеспечение тканей больных COVID-19
09.09.2021Источник: Kulow Vera A., Fähling Michael,
How to increase cellular oxygen availability in COVID‐19?
Аннотация
Коронавирусная пандемия (COVID‐19) все еще держит мир в напряжении. Заражение острым респираторным синдромом coronavirus‐19 (SARS‐CoV‐2) ухудшает кислородную диффузионную способность легких и в последствии вызывает пониженную оксигенацию крови. В 20% ‐ 40% случаев COVID‐19, у пациентов имеется критически низкая кислородная (O2) насыщенность крови, при этом нет проявлений в виде одышки. Такое состояние получило название “тихая гипоксия”. Однако, пониженная оксигенация крови приводит к тяжелым повреждениям в разнообразных органах, особенно имеющих высокую кислородную зависимость, такие как мозг, сердечная или почечная ткань. Тканевая гипоксия возникает из-за дисбалланса между потреблением O2 и поставкой O2, что вынуждает клетки адаптироваться с помощью некоторых физиологических процессов, о чем было сообщено в Протоколах Physiologica (Oxf). В целом, но также и в контексте COVID‐19, основное понимание клеточной доступности O2 представляет какое количество кислорода, достигает клетки, или более точно митохондрий для окислительного метаболизма, в основном относится к а) переносимому объему кислорода в крови, и к уровню гемоглобина крови и б) способности к доставке O2 в ткани, и сродством связки Hb‐O2. Последнее может быть недостаточно изученным аспектом, недооцененным в клиническом формате, лишь немногие исследователи обращались к этой теме. Однако из-за риска тромботических осложнений, проблема сродства Hb‐O2 могла бы иметь исключительную важность при COVID‐19 и тихой гипоксии. Таким образом мы задаемся вопросом, может ли модуляция сродства кислорода к гемоглобину помочь улучшить клеточную кислородную доступность.
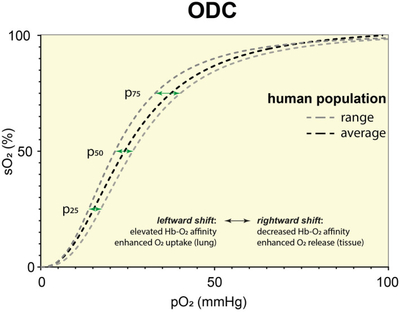
Сродство Hb‐O2 показано в кислородной кривой разобщения (ККР), показывая насыщенность O2 крови (sO2) при изменении парциальных давлений O2 (pO2). Имеются две важные особенности: Во-первых, его положение в полунасыщенном состоянии pO2, определенном как p50, который используется, чтобы описать сродство Hb‐O2 и во-вторых, ее кривая (n в логарифмическом участке Хилла) сродства Hb‐O2, смоделировано pCO2, pH (H + уровень), температурные и органические фосфаты, самое главное 2,3‐bisphosphoglycerate (2,3‐BPG, раньше 2,3‐DPG). Стандарт p50 у людей составляет 26.9 мм рт. ст. при pH 7.4 и 37°C. Каковы проявления уменьшения и увеличения этого показателя, указывающие на увеличенную или сниженную близость Hb‐O2 соответственно?
Левый сдвиг ККР (меньше p50) связан с улучшенной кислородной нагрузкой Hb в легочной системе. Например, дыхательные причины алкалоза увеличили сродство Hb‐O2 и, таким образом, улучшили кислородное обеспечение. Тем не менее, левый сдвиг ККР также связан с пониженным кислородным насыщением тканей. Правый сдвиг ККР улучшает клеточную кислородную доступность и происходит, например, при условиях повышенной физической нагрузки мышц. Здесь, увеличилось pCO2, H+, температура также вызывают изменение ККР вправо, гарантируя, что больше кислорода поступает при условиях более высоких кислородных потребностей. Кроме того, у беременных женщин высокий уровень сродства гемоглобина к кислороду и это помогает обеспечить плод кислородом. Эмбриональный гемоглобин, с другой стороны, не восприимчив к 2,3‐BPG и, из-за высокого сродства Hb‐O2, может хорошо поглотить материнский кислород. Между тем, высокая плотность капилляров также способствует высокому сродству Hb‐O2 у плода. Правое отклонение ККР также происходит при анемии и это компенсационный механизм, чтобы поддержать клеточную кислородную доступность.
В частности, в группе 60 молодых и здоровых людей, p50 показал поразительно высокое разнообразие, в пределах от 24.87 мм рт. ст. до 31.8 мм рт. ст., коррелировавших ниже или выше 2,3‐BPG уровни в крови соответственно. Таким образом высокое разнообразие p50, наблюдаемое в популяции представляет фундаментальное свойство, которое должно быть принято во внимание. Женщины, в среднем, показали более низкое сродство Hb‐O2, чем мужчины. Однако клеточная кислородная доступность, как ожидается, будет одинаковой, поскольку у мужчин наблюдается сродство Hb‐O2 с высоким объемом (уровень Hb) переносимогокислорода.
Так как различные болезни сопровождаются гипоксией, было бы полезно, изменить изначальное сродство Hb‐O2. Как упомянуто выше, сродство Hb‐O2 может быть смодулировано через различные эндогенные процессы. Водородные ионы, pCO2 и температура являются критическими определяющими факторами острой адаптации в сродстве Hb‐O2 во время повышенных физических нагрузок, но строго отрегулированы другими механизмами. Интересно, то, что анемия может появляться в результате COVID‐19, но как сообщают несколько исследований, опубликованных до сих пор, не указали ни на какую альтерацию p50. Таким образом, вопрос возникает, можем ли мы вызвать искусственную модуляцию сродства Hb‐O2.
В этом отношении более чем 50лет назад ученые начали искать синтетические модификаторы сродства Hb‐O2, специально для лечения Серповидно-клеточной анемии (SCD). Один из первых методов лечения был использование орального цианата натрия. Цианат взаимодействует и с альфа-цепями и с бета цепями остатков валина аминопласта в Hb, названный carbamylation, предотвращает появление серповидности эритроцитов. Лечившиеся пациенты показали уменьшение падения уровня гемолиза, билирубина и уровня лактатдегидрогеназы, а также увеличении Hb и резистентности эритроцитов к разрушению. Однако, дальнейшее использование у пациентов были остановлены из-за высокой токсичности цианата натрия. Чтобы избежать таких побочных эффектов, Deiderich и др. разработал метод экстракорпорального введения карбоамилата. Действительно, количество серповидных клеток при серповидноклеточной анемии было уменьшено на 65% без токсичных побочных эффектов цианата. Уровень p50 сдвинулся влево от 33 до 26 мм рт. ст., но что удивительно, из-за увеличенных уровней Hb у пациентов, доступная оксигенация увеличилась также. В целом, этот метод является очень сложным и трудноуправлямым, таким образом, дальнейшие расследования были отменены. За эти годы, было разработано много лекарств, которые способны взаимодействовать с Hb и сместить ККР влево, как 5‐hydroxymethyl‐2‐furfural (5‐HMF или AES‐103) и Voxelotor (GBT440).19, Оба вещества были разработаны для лечения серповидноклеточной анемии.
С другой стороны, чтобы лечить гипоксические состояния продолжаются исследования в области синтетических модуляторов Hb, смещающих ККР вправо. Например, Эфапроксирал или RSR‐13 (2 ‐ [4 ‐ [[(3,5‐dimethylanilino) карбонил] метил] phenoxyl] ‐2‐methylpropionic кислота) действует как аллостерический эффектор, который нековалентно связывается дезоксигенированным Hb, что приводит к уменьшению сродства Hb‐O2.
Каковы наши перспективы? Во-первых, это представляет интерес, чтобы знать, коррелирует ли высокий риск тяжелого течения COVID‐19 сродство Hb‐O2. Однако при улучшении сродства Hb‐O2 синтетическими модификаторами, может быть обеспечена оксигенация ткани.
КОНФЛИКТ ИНТЕРЕСОВ
Авторы объявляют, что нет никаких конфликтов интересов.
Ссылка: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8420209


